Клинический опыт применения топического изотретиноина в лечении акне папуло-пустулезной формы
© С.В. КЛЮЧАРЕВА1, А.В. КАРПОВА2,3, К.В. НОЗДРИН3
1 – ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия;
2 – ФГАОУ ВО «Российский университет дружбы народов», Москва, Россия;
3 – АО «Ретиноиды», Москва, Россия.
Резюме
Высокая распространенность акне во всем мире и в России в том числе, влияние, которое оказывает это заболевание на качество жизни пациентов, роль многочисленных факторов внешней среды, особенностей питания и образа жизни на течение болезни определяют актуальность повышения эффективности ее лечения и непрерывного поиска доступных, удобных в применении и безопасных лекарственных средств.
Цель исследования. Продемонстрировать высокую эффективность и безопасность раствора, содержащего 0,025% изотретиноина в спиртогликолевой основе, у пациентов с акне папуло-пустулезной формы.
Материалы и методы. Под наблюдением находились 88 пациентов с акне папуло-пустулезной формы в возрасте от 18 до 47 лет. В 1-й группе (n=48) пациентам назначали наружно препарат, содержащий 0,025% изотретиноина 1—2 раза в день в течение 4—6 нед. Пациенты 2-й группы (n=40) получали наружную терапию кремом, содержащим 0,1% адапалена, по инструкции, общей продолжительностью до 12 нед.
Результаты и вывод: Через 12 нед количество папул и пустул у пациентов 1-й группы стало меньше, чем у пациентов 2-й группы (p<0,001), причем достоверную разницу относительно исходного значения наблюдали в каждой точке наблюдения (p<0,001) на протяжении всего курса лечения. При оценке глобального терапевтического эффекта (ГОТЭ) получены достоверные положительные результаты: уже на 30-й день лечения в 1-й группе половина пациентов отметили хорошую эффективность препарата — 2,1 балла, а через 90 дней практически все оценили терапевтическую эффективность в 2,9 балла против 1,9 и 2,1 балла во 2-й группе.
Ключевые слова: акне, папуло-пустулезная форма, топический изотретиноин, 13-цис-ретиноевая кислота, спиртогликолевая основа.
Информация об авторах:
Ключарева С.В. — https://orcid.org/0000-0003-0801-6181
Карпова А.В. — https://orcid.org/0000-0003-4528-1013
Ноздрин К.В. — https://orcid.org/0000-0002-2943-3585
Введение
Высокая распространенность акне во всем мире и в России в том числе, влияние, которое оказывает это заболевание на качество жизни пациентов, роль многочисленных факторов внешней среды, особенностей питания и образа жизни на течение болезни определяют актуальность повышения эффективности ее лечения и непрерывного поиска доступных, удобных в применении и безопасных лекарственных средств [1—4].
По данным Американской академии дерматологии, только в США более 50 млн человек страдают акне в той или иной форме, преимущественно это подростки и молодые люди, но также наблюдается акне у взрослых (acne tarda) [1]. Изучение патогенеза заболевания позволяет выделить несколько ключевых звеньев: гиперсекреция кожного сала, фолликулярный гиперкератоз, колонизация Cutibacterium acnes (ранее Propionibacterium acnes), а также сложные воспалительные механизмы, обусловленные иммунными реакциями [1, 4, 5]. Соответственно препараты, назначаемые пациентам с акне, должны уменьшать излишнюю секрецию кожного сала, нормализовывать процесс ороговения клеток, снижать концентрацию C. acnes и влиять на воспалительный процесс.
Выбор терапии для пациентов с акне обусловлен клинической формой и тяжестью заболевания, типом кожи, полом, возрастом, сопутствующими заболеваниями и эффективностью предшествующего лечения [1, 6, 7]. С учетом клинической картины заболевания выделяют комедональные, папуло-пустулезные, узловатые и конглобатные акне, а также легкую, среднюю и тяжелую степени тяжести [1, 7]. При комедональных и папуло-пустулезных акне легкой и средней степени тяжести российскими и зарубежными сообществами рекомендована наружная терапия, преимущественно топическими ретиноидами, в виде монотерапии или в комбинациях с наружными антибактериальными препаратами [1, 7, 8].
Топические ретиноиды — производные витамина A, которые связываются с различными ядерными рецепторами ретиноевой кислоты и оказывают на кожу комедолитическое, себостатическое, противовоспалительное и регенерирующее действие, нормализуют процессы кератинизации и эпидермальной дифференцировки [8—11]. В настоящее время на рынке РФ ретиноиды для местного применения представлены синтетическим аналогом ретиноевой кислоты (ретиноидоподобное соединение) — адапаленом, в том числе в комбинациях с бензоила пероксидом, клиндамицином и метронидазолом (Франция, Швейцария, Индия, Россия), и биологически активной формой витамина A — изотретиноином (Россия) [12]. С учетом распространенности заболевания в молодом возрасте представляется важным наличие ассортимента доступных, бюджетных лекарственных средств для наружной терапии, содержащих ретиноиды, таких как Ретиноевая мазь и Ретасол.
Ретасол представляет собой раствор, содержащий 0,025% изотретиноина в спиртогликолевой основе. Изотретиноин (13-цис-ретиноевая кислота) тормозит терминальную дифференцировку себоцитов, гиперпролиферацию эпителия выводных протоков сальных желез, уменьшает выработку кожного сала, нормализует его состав и облегчает его эвакуацию, снижает воспалительную реакцию вокруг желез. Этиловый спирт, входящий в состав Ретасола, оказывает обезжиривающее, антисептическое и дополнительное комедонолитическое действие, что повышает общий фармакологический эффект препарата [13].
Раствор показан взрослым и подросткам старше 12 лет с папуло-пустулезной и комедональной формами акне. Его также применяют в лечении розацеа (при небольшом количестве высыпаний), периорального и себорейного дерматита. Раствор наносят ватным тампоном на предварительно очищенную кожу (после умывания или протирания тоником, не содержащим алкоголя) 2 раза в день. Продолжительность лечения от 4 до 12 нед.
Цель исследования — продемонстрировать высокую эффективность и безопасность препарата Ретасол у пациентов с акне папуло-пустулезной формы.
Материал и методы
Под наблюдением находились 88 пациентов с акне папуло-пустулезной формы, из них 18 (20,5%) мужчин и 70 (79,5%) женщин в возрасте от 18 до 47 лет. Продолжительность заболевания составила от нескольких месяцев до 7 лет. Распределение по степени тяжести заболевания: легкая у 33 (37,5%) пациентов (рис. 1), средняя у 34 (38,6%) (рис. 2), тяжелая у 21 (23,9%) (рис. 3). У всех пациентов высыпания носили распространенный характер с локализацией на коже лица, груди и верхней части спины.
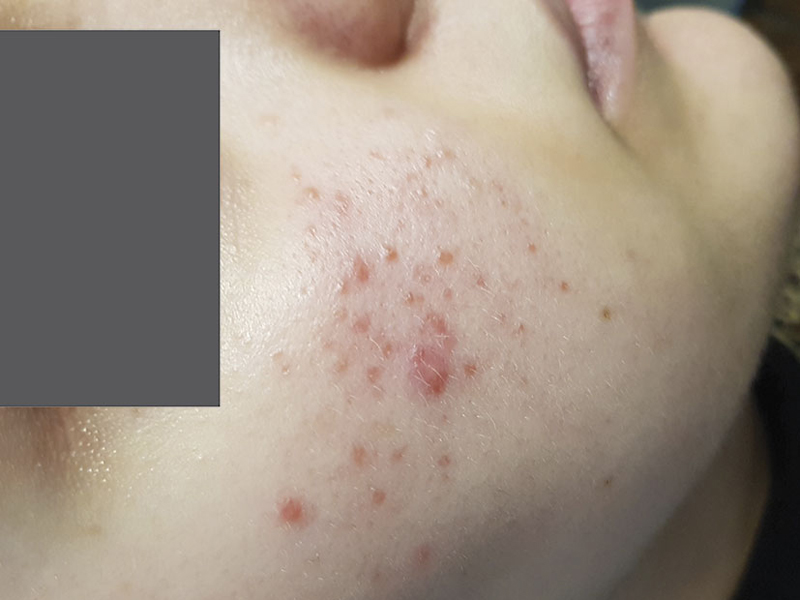
Рис 1. Пациентка Е., 19 лет. Начало заболевания с 18 лет. Диагноз: «акне легкой формы»
В области лица присутствуют единичные папулы и пустулы. В анамнезе — лечение косметическими средствами, без эффекта.
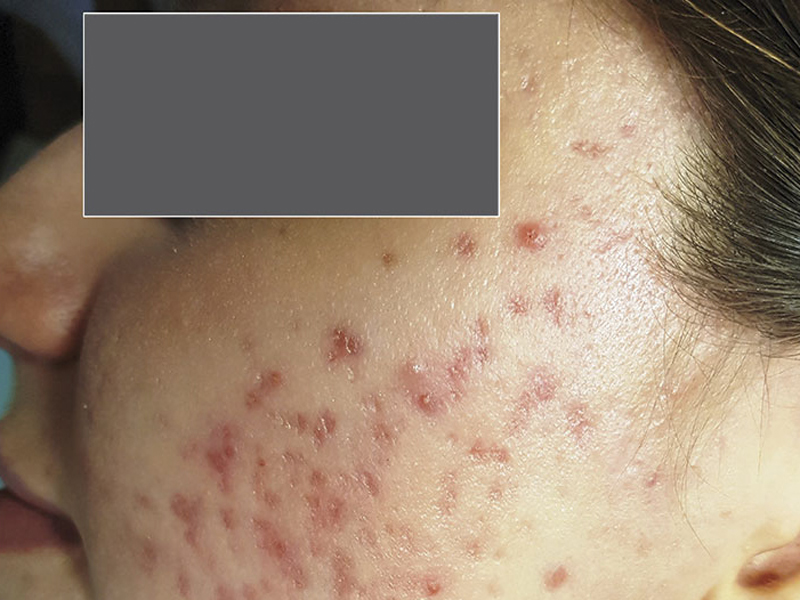
Рис 2. Пациентка К., 27 лет. Начало заболевания с 22 лет. Диагноз: «акне средней формы».
Заболевание рецидивировало ежемесячно, в анамнезе имеется заболевание органов ЖКТ и ЛОР-органов. В области лица присутствуют единичные папулы, множественные пустулы и атрофические рубцы.
Пациенты разделены на две группы таким образом, чтобы соотношение степеней тяжести болезни в каждой группе было одинаковым. В 1-й группе (n=48) пациентам назначили наружно Ретасол 1—2 раза в день на протяжении 4—6 нед. По мере регресса высыпаний и уменьшения жирности кожи пациентам назначали Ретиноевую мазь 0,1% для наружного применения 1—2 раза в день общей продолжительностью до 6—8 нед. В дальнейшем для поддержания эффекта рекомендовали использовать Ретиноевую мазь 0,05% 1 раз в день общей продолжительностью до 6 мес.
Пациенты 2-й группы (n=40) получали наружную терапию кремом, содержащим 0,1% адапалена, по инструкции, общей продолжительностью до 12 нед.
Критерии исключения: наличие в анамнезе аллергических реакций на компоненты препаратов, противопоказаний к применению, общее тяжелое состояние пациента, обусловленное соматической патологией, не позволяющее пациенту соблюдать необходимый режим, отсутствие готовности к сотрудничеству со стороны пациента, невозможность соблюдать условия протокола.
В целях предотвращения возможных побочных действий пациентам рекомендовали проверять переносимость препаратов на отдельном участке кожи (шея), избегать инсоляции, не использовать в период лечения сульфаниламиды и производные фенотиазина.
Эффективность и переносимость терапии оценивали 1 раз в месяц на протяжении 12 нед, что предусматривало оценку данных клинического осмотра и субъективных ощущений (жалоб) пациентов, фотографирование, подсчет количества воспалительных элементов (папулы и пустулы), оценку дерматологического индекса качества жизни (шкала ДИКЖ), глобальную оценку терапевтического эффекта (ГОТЭ) с применением метода ранжирования в баллах (3 балла — отличный результат, 2 — хороший, 1 — удовлетворительный, 0 — неудовлетворительный). Отдаленные результаты оценивали через 12 мес от начала лечения.
Статистическая обработка данных выполнена с использованием пакетов прикладных программ Statistica 10. Для определения динамики количества воспалительных элементов проведен ранговый дисперсионный анализ по Фридману, рассчитан показатель убыли (прироста) количества воспалительных элементов в процентах к исходному уровню по среднегрупповым значениям.
Исследование одобрено локальным этическим комитетом.
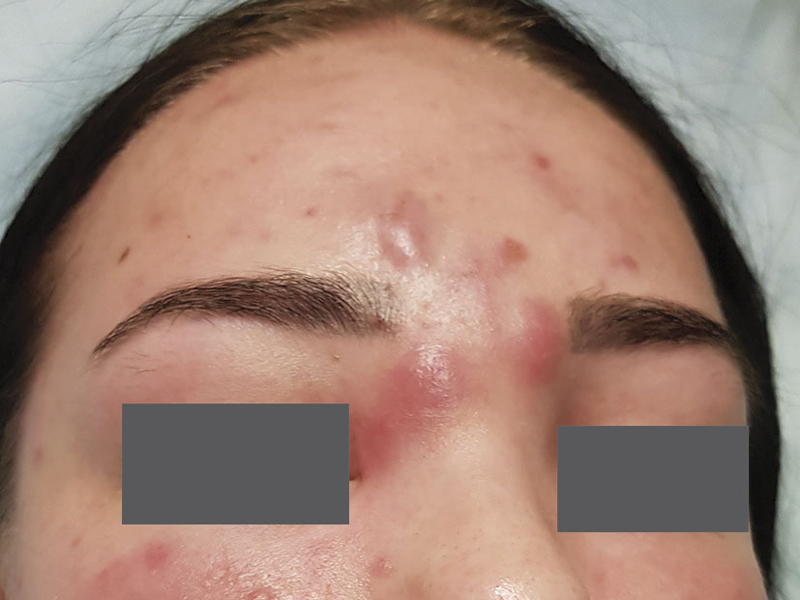
Рис 3. Пациентка А., 24 года. Начало заболевания с 17 лет. Диагноз: «акне среднетяжелой формы».
Процесс на коже в виде закрытых комедонов носил длительный характер, но обострение возникло относительно остро, в течение полугода появились папулы и пустулы на лице, сформировались болезненные конглобаты в области переносицы и лба, которые сохранялись в течение 3 мес. В анамнезе — заболевания эндокринной системы и нарушение менструального цикла. В области лица присутствуют единичные папулы, множественные пустулы, в лобной части инфильтраты, плотные.
Результаты
Изначально сформированные группы пациентов были однородны по выраженности воспалительного процесса (рпапулы=0,65; рпустулы=0,88). Через 12 нед количество папул и пустул в 1-й группе стало меньше по сравнению со 2-й группой (p<0,001), причем достоверную разницу относительно исходного значения наблюдали в каждой точке наблюдения (p<0,001) на протяжении всего курса лечения. Оценка количества воспалительных элементов до, в процессе и после окончания лечения представлена в табл. 1 и на рис. 4—9.
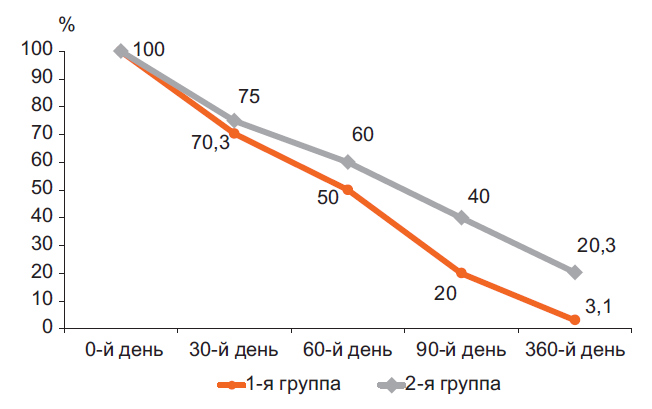
Рис 4. Уменьшение количества папул в процессе лечения.
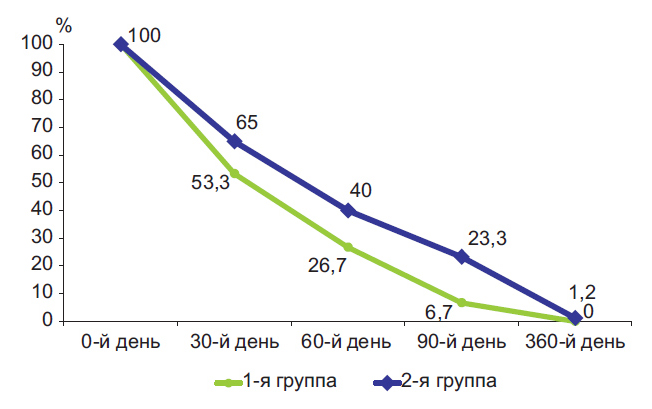
Рис 5. Уменьшение количества пустул в процессе лечения.
Как видно из табл. 1, уже в конце первого месяца лечения отмечалась значительная положительная динамика: уменьшение папул на 29,7 и 25% и пустул на 46,7 и 35% в 1-й и 2-й группах соответственно. Через 12 нед наблюдали уменьшение папул на 80 и 60% и пустул на 93,3 и 76,7%.
| День лечения | 1-я группа (n=48) | 2-я группа (n=40) | ||||||
|---|---|---|---|---|---|---|---|---|
| Папулы | Пустулы | Папулы | Пустулы | |||||
| абс. | % | абс. | % | абс. | % | абс. | % | |
| 0-й (до лечения) | 960 | 100 | 720 | 100 | 800 | 100 | 600 | 100 |
| 30-й | 675 | 70,3 | 384 | 53,3 | 600 | 75,0 | 390 | 65,0 |
| 60-й | 480 | 50,0 | 192 | 26,7 | 480 | 60,0 | 240 | 40,0 |
| 90-й (12 нед) | 192 | 20,0 | 48 | 6,7 | 320 | 40,0 | 140 | 23,3 |
| 360-й | 30 | 3,1 | 0 | 0 | 162 | 20,3 | 7 | 1,2 |
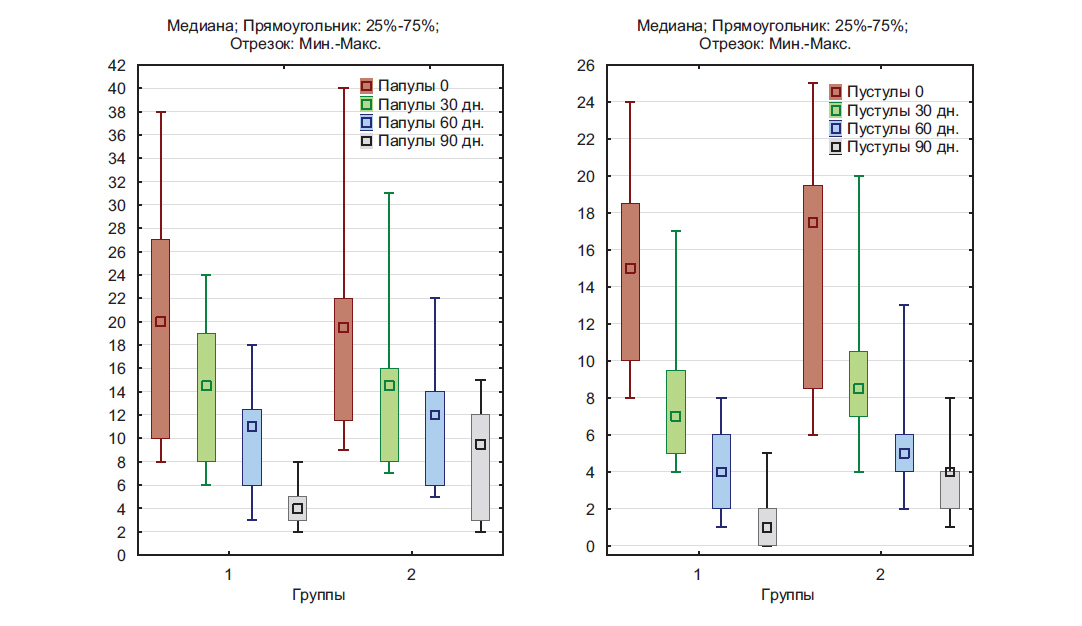
Рис 6. Гистограмма медиан количества воспалительных элементов.
| Раздел | Баллы мах | Группы сравнения | Значимость различий при сравнении групп | ||||||
|---|---|---|---|---|---|---|---|---|---|
| 1-я группа (n=48) | 2-я группа (n=40) | pдо | pпосле | ||||||
| до | после | p | до | после | p | ||||
| 1. Симптомы и ощущения | 5 | 2,3±1,2 | 1,1±0,4 | <0,001 | 2,3±1,3 | 1,6±1,1 | <0,001 | 1,0 | 0,0096 |
| 2. Ежедневная деятельность | 3 | 2,1±0,8 | 1,2±0,5 | <0,001 | 1,8±0,7 | 1,2±0,4 | <0,001 | 0,060 | 0,90 |
| 3. Отдых (досуг) | 3 | 1,6±0,6 | 0,8±0,5 | <0,001 | 1,5±0,6 | 1,3±0,5 | <0,001 | 0,67 | <0,001 |
| 4. Работа и учеба | 3 | 1,4±0,6 | 0,7±0,5 | <0,001 | 1,4±0,6 | 0,8±0,5 | <0,001 | 0,84 | 0,47 |
| 5. Межличностные отношения | 5 | 3,2±1,1 | 1,2±0,6 | <0,001 | 3,2±1,1 | 2,5±1,3 | <0,001 | 0,89 | <0,001 |
| Сумма баллов | - | 10,4±3,3 | 5,0±2,2 | <0,001 | 10,1±3,3 | 7,4±2,9 | <0,001 | 0,68 | <0,001 |
| 6. Эффективность лечения — ГОТЭ | 3 | 2,2±0,8 | 3,0±0,2 | <0,001 | 2,0±0,7 | 2,2±0,5 | 0,0034 | 0,16 | 0,0000 |
Примечание: p — значимость критерия Стьюдента для связанных выборок при сравнении показателей до и после лечения в каждой из групп; pдо — зна- чимость критерия Стьюдента для независимых групп при сравнении показателей в 1-й и 2-й группах до лечения, pпосле — после лечения.
Наблюдение отдаленных результатов через 12 мес от начала лечения продемонстрировало высокую эффективность проведенной терапии с переходом в длительную клиническую ремиссию: наблюдалось уменьшение папул на 96,9 и 79,7% и пустул на 100 и 98,8% в 1-й и 2-й группах соответственно. В 1-й группе регресс высыпаний сохранялся у 97% пациентов, во 2-й — у 77% (см. рис. 4—9).
Анализ данных осмотров и жалоб пациентов позволил оценить переносимость терапии в обеих группах. Необходимо отметить, что наружное применение ретиноидов всегда сопровождается дерматологическими реакциями (раздражительный дерматит), которые не требуют специфической терапии и в большинстве случаев проходят самостоятельно после коррекции режима дозирования и применения увлажняющих косметологических средств. К оцениваемым параметрам (симптомы и жалобы) относились чувство жжения (покалывания), зуд, гиперемия, отечность и сухость кожи.
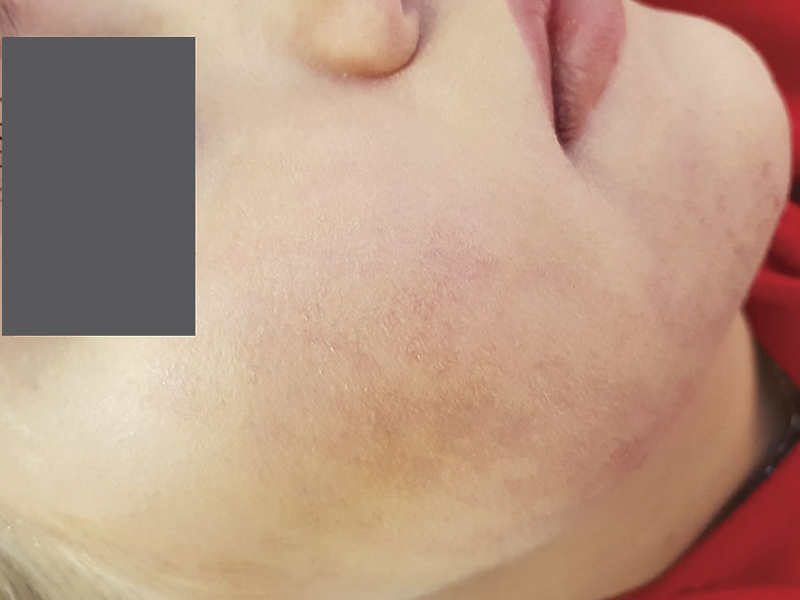
Рис 7. Пациентка Е., 19 лет. Через 1 мес после терапии препаратом Ретасол 2 раза в день. Эффективность лечения составила 90%.
Во время визита через 1 мес после начала лечения усиление чувства жжения отметили 6,2 и 7,5% пациентов в 1-й и 2-й группах соответственно, повышение сухости кожи — 22,9 и 32,5%, усиление зуда — 4,1 и 10%, усиление отечности — 2,1 и 2,5%. При этом наблюдали уменьшение гиперемии у 25,1 и 27,5% пациентов в 1-й и 2-й группах соответственно.
В конце 12-недельного курса лечения побочные явления в виде чувства жжения, зуда, отека были незначительные, соответственно 4,1; 10,4; 4,1% в 1-й группе и 5,0; 17,5; 5,0% во 2-й. Сухость кожи к концу лечения сохранялась у 8,2 и 12,5% пациентов в 1-й и 2-й группах соответственно, что демонстрирует лучшую переносимость в 1-й группе.
Анализ силы влияния использованных методов лечения на качество жизни пациентов в группах по результатам ДИКЖ до и после лечения и ГОТЭ (M±p) представлен в табл. 2. При оценке глобального терапевтического эффекта (ГОТЭ) получены достоверные положительные результаты: уже на 30-й день лечения в 1-й группе половина пациентов отметили хорошую эффективность препарата — 2,1 балла, а через 90 дней практически все оценили терапевтическую эффективность на 2,9 балла, против 1,9 и 2,1 балла во 2-й группе.
Оценка показателей качества жизни пациентов по результатам лечения продемонстрировала существенно большую выраженность положительного влияния терапии в 1-й группе по сравнению со 2-й, данные представлены в табл. 3.
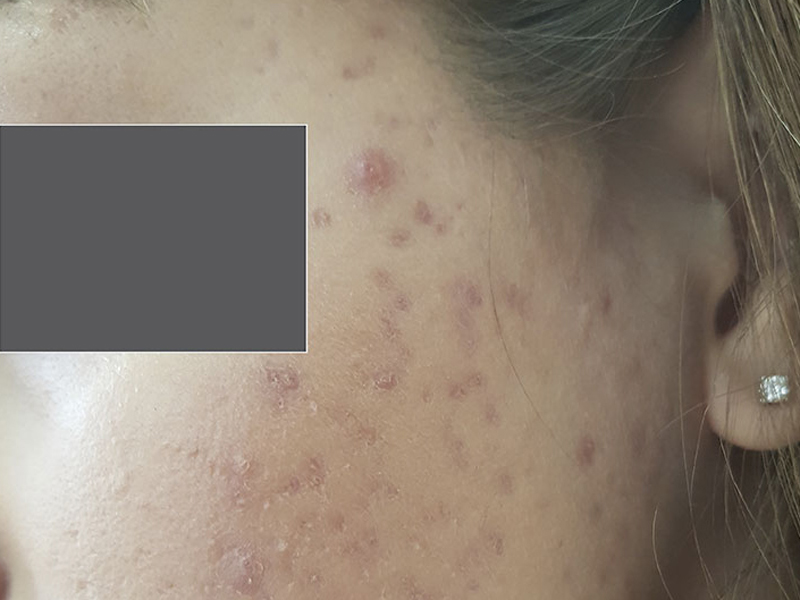
Рис 8. Пациентка К., 27 лет. Через 1 мес после терапии препаратом Ретасол 2 раза в день. Эффективность лечения составила 80%.
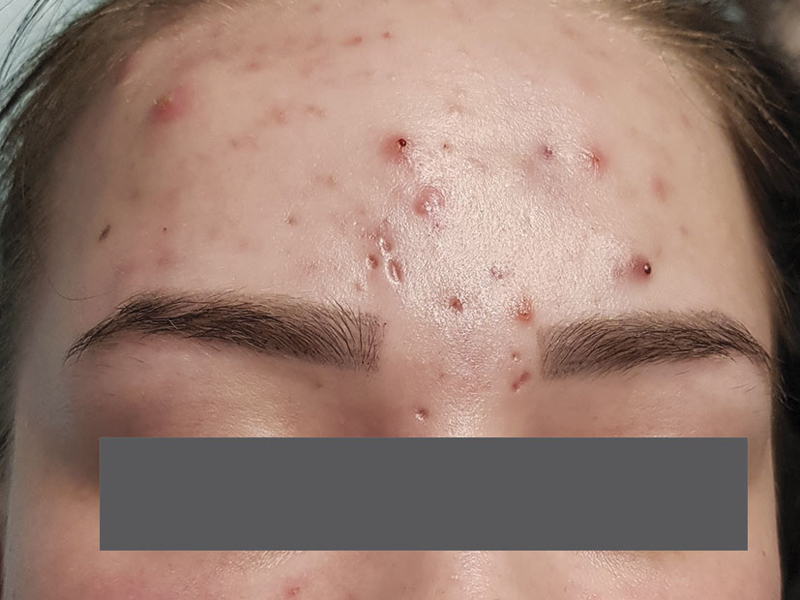
Рис 9. Пациентка А., 24 года. Через 1 мес после терапии прапаратом Ретасол 2 раза в день. Эффективность лечения составила 80% (папулы и пустулы разрешились, размер инфильтратов уменьшился).
| Показатель | 1-я группа | 2-я группа |
|---|---|---|
| Симптомы и ощущения: | ||
| до лечения | 2 (1; 3) | 2 (1; 3) |
| после лечения | 1 (1; 1) | 1 (1; 2) |
| Ежедневная деятельность: | ||
| до лечения | 2 (2; 3) | 2 (1; 2) |
| после лечения | 1 (1; 1) | 1 (1; 1) |
| Отдых (досуг): | ||
| до лечения | 2 (1; 2) | 1 (1; 2) |
| после лечения | 1 (0; 1) | 1 (1; 1) |
| Работа и учеба: | ||
| до лечения | 1 (1; 2) | 1 (1; 2) |
| после лечения | 1 (0; 1) | 1 (0; 1) |
| Межличностные отношения: | ||
| до лечения | 3 (3; 4) | 3 (3; 4) |
| после лечения | 1 (1; 1) | 2 (1; 3) |
| Эффективность лечения: | ||
| на 30-й день | 2 (2; 3) | 2 (2; 2) |
| на 90-й день | 3 (3; 3) | 2 (2; 2) |
Наибольший статистический разброс отмечается по показателям «симптомы и ощущения» как в 1-й, так и во 2-й группе. Вместе с тем отмечена более выраженная динамика улучшения показателей качества жизни пациентов в 1-й группе по сравнению со 2-й, прежде всего по такому параметру, как межличностные отношения (снижение с 3 (3; 4) до 1 (1; 1) балла), а также значительное увеличение показателя «эффективность лечения» с 2 (2; 3) до 3 (3; 3) баллов.
После окончания курса лечения анализ качества жизни пациентов продемонстрировал уменьшение всех параметров в обеих группах: по сумме баллов в 1-й группе до лечения показатель составил 10,4 балла, через 90 дней — 5 баллов, что позволило пациентам существенно улучшить межличностные отношения, повысить эффективность трудовой деятельности и учебы. Во 2-й группе эти показатели составили 10,1 и 6,1 балла соответственно. Таким образом, ДИКЖ в 1-й группе улучшился на 52%, а во 2-й — на 40%, что говорит о положительном влиянии терапии на качество жизни пациентов. При этом в 1-й группе показатели оказались выше на 12%.
Заключение
Полученные в ходе исследования результаты демонстрируют высокую эффективность и переносимость препарата Ретасол в лечении акне папуло-пустулезной формы. Побочные явления в виде зуда, жжения, отека, гиперемии и сухости кожи были незначительными и менее выраженными, чем во 2-й группе.
Стойкая, длительная клиническая ремиссия и значительное повышение качества жизни пациентов позволяет рекомендовать данный препарат в качестве доступного, бюджетного, высокоэффективного средства для лечения акне в качестве монотерапии или комбинированной терапии совместно с Ретиноевой мазью по схеме: наружно Ретасол 1—2 раза в день в течение 4—6 нед, затем наружно Ретиноевая мазь 0,1% 1—2 раза в день общей продолжительностью до 6—8 нед, затем наружно Ретиноевая мазь 0,05% 1 раз в день до 6 мес для поддержания эффекта.
Литература
- Zaenglein AL, Pathy AL, Schlosser BJ, Alikhan A, Baldwin HE, Berson DS, Bowe WP, Graber EM, Harper JC, Kang S, Keri JE, Leyden JJ, Reynolds RV, Silverberg NB, Stein Gold LF, Tollefson MM, Weiss JS, Dolan NC, Sagan AA, Stern M, Boyer KM, Bhushan R. Guidelines of care for the management of acne vulgaris. J Am Acad Dermatol. 2016;74(5):945-973.e33. Epub 2016 Feb 17. Erratum in: J Am Acad Dermatol. 2020;82(6):1576. PMID: 26897386.
- Kucharska A, Szmurło A, Sińska B. Significance of diet in treated and untreated acne vulgaris. Postepy Dermatol Alergol. 2016;33(2):81-86. Epub 2016 May 16. PMID: 27279815; PMCID: PMC4884775.
- Cooper AJ, Harris VR. Modern management of acne. Med J Aust. 2017;206(1):41-45. PMID: 28076744.
- Li X, He C, Chen Z, Zhou C, Gan Y, Jia Y. A review of the role of sebum in the mechanism of acne pathogenesis. J Cosmet Dermatol. 2017;16(2):168-173. Epub 2017 May 29. PMID: 28556292.
- Platsidaki E, Dessinioti C. Recent advances in understanding Propionibacterium acnes (Cutibacterium acnes) in acne. F1000Res. 2018;7:F1000 Faculty Rev-1953. PMID: 30613388; PMCID: PMC6305227.
- Gollnick HP, Bettoli V, Lambert J, Araviiskaia E, Binic I, Dessinioti C, Galadari I, Ganceviciene R, Ilter N, Kaegi M, Kemeny L, López-Estebaranz JL, Massa A, Oprica C, Sinclair W, Szepietowski JC, Dréno B. A consensusbased practical and daily guide for the treatment of acne patients. J Eur Acad Dermatol Venereol. 2016;30(9):1480-1490. Epub 2016 May 14. PMID: 27177989.
- Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 5-е изд., перераб. и доп. М.: Деловой экспресс; 2016;9-27.Federal’nye klinicheskie rekomendatsii. Dermatovenerologiya 2015: Boleznikozhi. Infektsii, peredavaemye polovym putem. 5-e izd., pererab. i dop. M.: Delovoi ekspress; 2016;9-27. (In Russ.).
- Nast A, Dréno B, Bettoli V, Bukvic Mokos Z, Degitz K, Dressler C, Finlay AY, Haedersdal M, Lambert J, Layton A, Lomholt HB, López-Estebaranz JL, Ochsendorf F, Oprica C, Rosumeck S, Simonart T, Werner RN, Gollnick H. European evidence-based (S3) guideline for the treatment of acne — update 2016 — short version. J Eur Acad Dermatol Venereol. 2016; 30(8):1261-1268. PMID: 27514932.
- Kolli SS, Pecone D, Pona A, Cline A, Feldman SR. Topical Retinoids in Acne Vulgaris: A Systematic Review. Am J Clin Dermatol. 2019;20(3):345-365. PMID: 30674002.
- Latter G, Grice JE, Mohammed Y, Roberts MS, Benson HAE. Targeted Topical Delivery of Retinoids in the Management of Acne Vulgaris: Current Formulations and Novel Delivery Systems. Pharmaceutics. 2019;11(10):490. PMID: 31554188; PMCID: PMC6835300.
- Yeh L, Bonati LM, Silverberg NB. Topical retinoids for acne. Semin Cutan Med Surg. 2016;35(2):50-56. PMID: 27416308.
- https://grls.rosminzdrav.ru
- Burylina OM, Karpova AV. Kosmetologiya. Klinicheskoye rukovodstvo. M. 2019;83, 114-115.