Влияние мази «Стизамет» на заживление ожоговых ран у крыс в стандартных условиях
Резюме
В статье представлены результаты изучения влияния мази «Стизамет»® на заживление ожоговых ран в стандартных условиях у крыс.
Цель ‒ изучить влияние мази «Стизамет»® на заживление ожоговых ран у крыс в стандартных условиях.
Материалы и методы. Исследование проводили на 40 крысах-самцах линии Wistar массой 110‒120 г. Для создания модели ожоговой раны использовали медный куб площадью основания 4 см2. Куб нагревали в кипящей воде и прикладывали к депилированному участку кожи межлопаточной области спины наркотизированных животных, вызывая ожог II степени. Со следующего дня (кроме крыс интактной группы) животным наносили основу или мазь «Стизамет»® до полного заживления раны у животных последней группы, при этом учитывали размер раны. В гистологических препаратах подсчитывали толщину клеточного эпидермиса.
Результаты и вывод: c 9-го дня эксперимента мазь «Стизамет»® стимулировала заживление ожоговых ран у крыс.
Ключевые слова: крысы, ожоговые раны, мазь «Стизамет»®
Введение
Мазь «Стизамет»® была зарегистрирована в качестве лекарственного средства в 2005 г. К этому времени был написан обзор литературы [1], изучены ее дерматотропная активность [2], фармакокинетика [3], безвредность [4], накоплен опыт применения мази в дерматологии [5] и хирургии [6]. Лечение ожогов II степени давало положительный результат на 8‒10-й дни после 3-кратной смены повязок. Однако у большинства пациентов (с ожогами III степени) терапевтическое действие препарата затягивалось до 28‒30 суток. Терапевтический эффект длительно незаживающих ран оказался малоэффективным. В целом, терапия была на 1‒2 дня короче в сравнении с традиционным курсом [7]. Проведенное позже поисковое исследование на крысах показало, что мазь «Стизамет»® в сравнении с другими композициями оказывает большее ранозаживляющее действие на ожоговые раны [8].
Целью настоящего исследования стало изучение влияния мази «Стизамет»® на заживление ожоговых ран у крыс в стандартных условиях.
Материалы и методы
Исследование проведено на 40 крысах-самцах линии Wistar массой 110‒120 г, полученных из питомника «Андреевка» филиала ФГБУН «МЦБ МТ» ФМБА России. Дополнительно 2 крысы были отправлены в лабораторию на предмет инфицирования. Правила содержания и ухода за животными выполнялись в соответствии с СОП АО «Ретиноиды». Замену клеток с подстилом и бутылками с водой производили 1 раз в 2 дня, влажную уборку – ежедневно. В качестве подстила использовали древесную стружку, полученную от ООО «Лабораторкорм» (Россия). Животные находились в карантине 14 суток в помещении с контролируемыми условиями окружающей среды по 8 крыс в поликарбонатных клетках. Крысы в группы подбирались случайным образом и, как и клетки, были промаркированы. Корм (поставщик ‒ «Лабораторкорм», Россия) соответствовал ГОСТ 55453-2013. Вода для питья проходила фильтрационную очистку. Корм и воду давали ad libitum. При поступлении животных осматривал ветеринарный врач. Больных крыс выбраковывали. Сведения о составе мазевой основы и мази «Стизамет»® представлены в табл. 1.
| Мазевая основа | |
|---|---|
| Описание – однородная мазь белого цвета | |
| Вспомогательные вещества | |
| Воск эмульсионный | 8,0 |
| Масло вазелиновое | 8,0 |
| Глицерин | 10,0 |
| Этанол 95% | 10,0 |
| Вода очищенная | до 100 г |
| Мазевая основа произведена в технологической лаборатории АО «Ретиноиды» | |
| «Стизамет»®, мазь для наружного применения | |
| Описание – однородная мазь белого цвета | |
| Диоксометилтетрагидропиримидин (метилурацил) | 3,0 |
| Воск эмульсионный | 8,0 |
| Масло вазелиновое | 8,0 |
| Этанол 95% | 10,0 |
| Вода очищенная | до 100 г |
| Препарат произведен АО «Ретиноиды». Серийный образец. | |
Мазевая основа и мазь «Стизамет»® были упакованы в стандартные алюминиевые тубы с внутренним лаковым покрытием (ТУ 9467‒001‒10010399‒2013) по 35 г, промаркированы и переданы для проведения эксперимента. Все манипуляции по получению, хранению, выдаче, учету, подготовке доз и уничтожению остатков основы и мази «Стизамет»® выполнялись в соответствии с СОП Центра доклинических исследований АО «Ретиноиды». Неиспользованные остатки мазевой основы и мази «Стизамет»® утилизировались. Предварительно крыс вводили в золетиловый наркоз (Вирбак, Франция) [10]. К депилированной коже межлопаточной области спины крысы прикладывали куб, выдержанный в кипящей воде, на 10 сек. [8], что вызывало ожог II степени (разрушение эпидермиса, умеренный отек дермы, слабый отек гиподермы). Со следующего дня (кроме крыс интактной группы) животным наносили мазевую основу или мазь «Стизамет»® до полного заживления раны у всех крыс группы. Навески препарата «Стизамет»® в количестве 0,05 г отвешивали на электронных весах АХ 120 (Япония). О заживлении судили по изменению среднего полудиаметра раны. По окончании эксперимента животных подвергли эвтаназии на установке АЕ 904 000 (Россия). Кожу из мест нанесения мазевой основы или мази «Стизамет»® готовили к гистологическому исследованию по традиционной методике [11]. Для подсчета толщины клеточного эпидермиса использовали микроскоп Аксиостар-плюс, оснащенный цифровым комплексом «Микромед-2-1600-3» (Германия) и программным обеспечением «Диаморф» (Россия). Материалы обрабатывали статистически [9]. Письменный план 004/20 БЭК утвержден 28.05.2020.
Результаты
Из представленных сведений (рис. и табл. 2) можно видеть, что с 9-го дня и до конца эксперимента достоверно возрастало различие в заживлении ожоговых ран у крыс, получивших местно мазь «Стизамет»®. При этом толщина клеточного эпидермиса также возрастала (табл. 3).
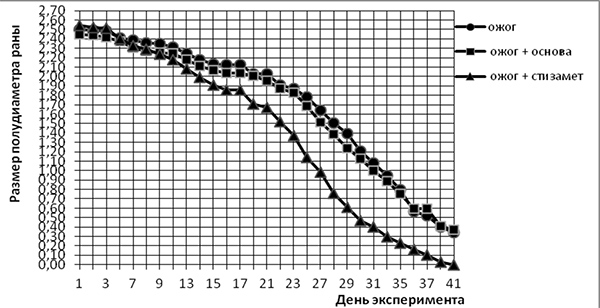
Рис. Динамика средних значений полудиаметра ожоговой раны у крыс линии Wistar, получавших местно мазь «Стизамет»®, в сравнении с такими же крысами, получавшими мазевую основу (в сантиметрах)
| День эксперимента | Значение t-критерия Стьюдента | Показатель различия |
|---|---|---|
| 1 | 0,80 | Не значимы |
| 2 | 0,71 | Не значимы |
| 3 | 0,35 | Не значимы |
| 6 | 0,20 | Не значимы |
| 7 | 1,20 | Не значимы |
| 8 | 1,65 | Не значимы |
| 9 | 2,20 | Значимы |
| 10 | 2,30 | Значимы |
| 13 | 2,74 | Значимы |
| 14 | 3,26 | Значимы |
| 15 | 3,43 | Значимы |
| 16 | 4,02 | Значимы |
| 17 | 4,02 | Значимы |
| 20 | 3,39 | Значимы |
| 21 | 3,82 | Значимы |
| 22 | 3,80 | Значимы |
| 23 | 4,70 | Значимы |
| 24 | 5,03 | Значимы |
| 27 | 5,11 | Значимы |
| 28 | 5,05 | Значимы |
| 29 | 4,99 | Значимы |
| 30 | 4,37 | Значимы |
| 31 | 3,69 | Значимы |
| 34 | 3,39 | Значимы |
| 35 | 3,21 | Значимы |
| 36 | 2,19 | Значимы |
| 37 | 2,40 | Значимы |
| 38 | 2,42 | Значимы |
| 41 | 2,62 | Значимы |
| Воздействие | № животного | М ± SE |
|---|---|---|
| Без воздействия | 1 | 2,7±0,37 |
| 2 | 3,5±0,57 | |
| 3 | 4,25±0,56 | |
| 4 | 4,36±0,8 | |
| 5 | 4,13±0,76 | |
| 6 | 4,36±0,92 | |
| 7 | 3,23±0,47 | |
| 8 | 3,60±0,46 | |
| М ± SE | 3,80 ± 0,47 | |
| Мазевая основа | 9 | 4,62±0,75 |
| 10 | 4,88±0,48 | |
| 11 | 4,49±0,58 | |
| 12 | 3,71±0,47 | |
| 13 | 3,91±0,48 | |
| 14 | 4,68±0,37 | |
| 15 | 3,68±0,68 | |
| 16 | 3,24±0,35 | |
| М ± SE | 4,16 ± 0,46 | |
| Ожог | 17 | 19,76±2,57 |
| 18 | 17,28±1,83 | |
| 19 | 19,07±1,53 | |
| 20 | 14,29±0,97 | |
| 21 | 11,84±0,99 | |
| 22 | 20,71±1,77 | |
| 23 | 34,57±4,94 | |
| 24 | 9,83±1,49 | |
| М ± SE | 18,42 ± 5,94 | |
| Ожог + мазевая основа | 25 | 12,46±1,17 |
| 26 | - | |
| 27 | 20,22±1,41 | |
| 28 | 10,77±1,14 | |
| 29 | 10,31±1,49 | |
| 30 | 14,73±0,79 | |
| 31 | - | |
| 32 | 6,05±1,19 | |
| М ± SE | 12,42 ± 4,57 | |
| Ожог + «Стизамет»® | 33 | 11,95±1,03 |
| 34 | 9,78±0,70 | |
| 35 | 13,97±1,76 | |
| 36 | 15,41±1,04 | |
| 37 | 10,04±1,20 | |
| 38 | 10,53±0,64 | |
| 39 | 9,42±0,60 | |
| 40 | 11,48±2,12 | |
| М ± SE | 11,57 ± 1,67 | |
Обсуждение
Проведенное исследование показало, что ожоговые раны кожи в стандартных условиях у крыс линии Wistar заживают быстрее, чем у аналогичных животных, получавших мазевую основу. Это отражено в графическом, статистическом и морфометрическом исследованиях. Замена мази «Стизамет»® на мазь Левомиколь небезупречна, т. к. эта мазь содержит помимо метилурацила левомицетин, неприменяемый для получения «косметического» рубца.
Вывод
Заживление ожоговой раны у крыс линии Wistar после местного применения мази «Стизамет»® начиналось с 9-го дня и завершалось к 41-му дню эксперимента, опережая таковое у животных контрольных групп.
Литература
- Белоусова Т.А. Фармакологические свойства метилурацила (обзор литературы) // Альманах «Ретиноиды». 2009. Вып. 28. С. 11‒43.
- Яцковский А.Н., Белоусова Т.А., Жучков С.А. и др. Дерматотропная активность мази Стизамет® // Альманах «Ретиноиды». 2009. Вып. 28. С. 43‒51.
- Ноздрин В.И., Гузев К.С., Архапчев Ю.П. Фармакокинетика метилурацила после аппликаций содержащих его мазей // Альманах «Ретиноиды». 2009. Вып. 28. С. 51‒57.
- Ноздрин В.И., Яцковский А.Н., Белоусова Т.А. и др. Изучение безвредности препарата Стизамет® // Альманах «Ретиноиды». 2009. Вып. 28. С. 57‒61.
- Альбанова В.И. Опыт применения мази Стизамет® в лечении аллергодерматозов и псориаза // Альманах «Ретиноиды». 2009. Вып. 28. С. 61‒68.
- Крастин О.А., Светухин А.М., Блатун Л.А. и др. Эффективность препарата Стизамет® при лечении ран мягких тканей // Альманах «Ретиноиды». 2009. Вып. 28. С. 71‒76.
- Смирнов С.В., Логинов Л.П., Шахламов М.В. Результаты клинического изучения мази Стизамет® при ожогах // Альманах «Ретиноиды». 2009. Вып. 28. С. 68‒71.
- Ноздрин К.В., Крот С.Л., Бородин В.В. и др. Влияние смеси ГЛС (ретинола пальмитат + метилурацил + декспантенол + хлоргексидина биглюконат) на ожоговые раны у крыс // Альманах «Ретиноиды». 2021. Вып. 36. С. 59‒64.
- Руководство по проведению доклинических исследований лекарственных средств / под ред. А.Н. Миронова. М.: Гриф и К, 2012. С. 51‒63.
- Вавилова В.А., Щекунова Е.В., Кашкин В.А. и др. Апробация метода оценки фототоксических эффектов лекарственных препаратов в условиях in vivo // Ведомости НЦ экспертизы средств медицинского применения. Т. 218. Вып. 2. С. 115‒122.